点击蓝字关注我们


世界首例猪肾移植人体成功
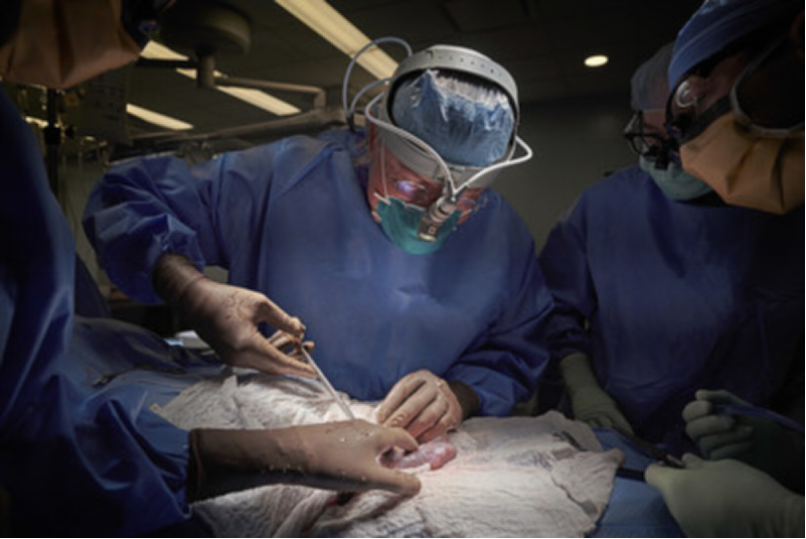
10月19日,美国纽约大学朗格尼医学中心移植外科教授Montgomery团队宣布,他们成功将α-Gal基因敲除的猪肾移植给了一名脑死亡者。移植术后,肾脏正常“工作”了54个小时,未发生超急性排异反应,患者尿液、肌酐水平降至正常。此次手术并不是将转基因猪的肾直接移植到人体内,而是附着在一例脑死亡受者的大腿上部、腹部外的血管上。据世界卫生组织统计,全世界每年大约有200万人需要器官移植,但器官供体面临严重短缺,全球平均器官供需比不足1:20。我国每年有超过30万人的器官出现衰竭,有移植手术需求,但受器官供体来源、经济条件、医疗条件的限制,每年仅有约1万人能够接受移植手术。此例手术成功具有重大里程碑意义,为将来的异种器官移植带来希望,有望解决目前供体短缺的问题。
异种移植的障碍1-4
异种移植后主要存在的障碍是移植后排斥反应、凝血问题、跨物种感染。其中主要的排斥反应为:(1)超急性排斥反应(HAR);(2)急性体液异种移植排斥反应(AHXR);(3)急性细胞排斥反应。
HAR为发生在24h之内的器官损伤,通常发生在数分钟和数小时之内,跟灵长类动物体内预存的抗猪抗体与猪动脉内皮细胞表面抗原的结合有关。引起超HAR的主要抗原为α-1,3-半乳糖抗原(a-Gal),由α-1,3-半乳糖转移酶(GGTA1)基因编码。这一寡糖存在于除人类和非人类灵长类动物(例如大猩猩、狒狒)之外的所有哺乳动物体内。这些灵长类物种在数百万年前由于基因突变丧失了α-1,3半乳糖基因的表达,从而导致了灵长类动物体内对抗a-Gal的抗体产生。引起HAR的抗原还有N-羟乙酰神经氨酸(NeuGc)和Sd(a)抗原,分别由胞苷单磷酸-N-乙酰神经氨酸羟化酶(CMAH)和β-1,4-N-乙酰半乳糖胺基转移酶(2b4GalNT2)基因编码。
AHXR是由体液和免疫细胞应答,结合活化的内皮和炎症共同引起的,一般发生在移植术后的数天或者数周以后。AHXR的组织病理学特征与HAR相似,还与抗体和补体沉积激活动脉内皮细胞,先天免疫细胞(如多核细胞、巨噬细胞、自然杀伤细胞)浸润摧毁移植器官有关。
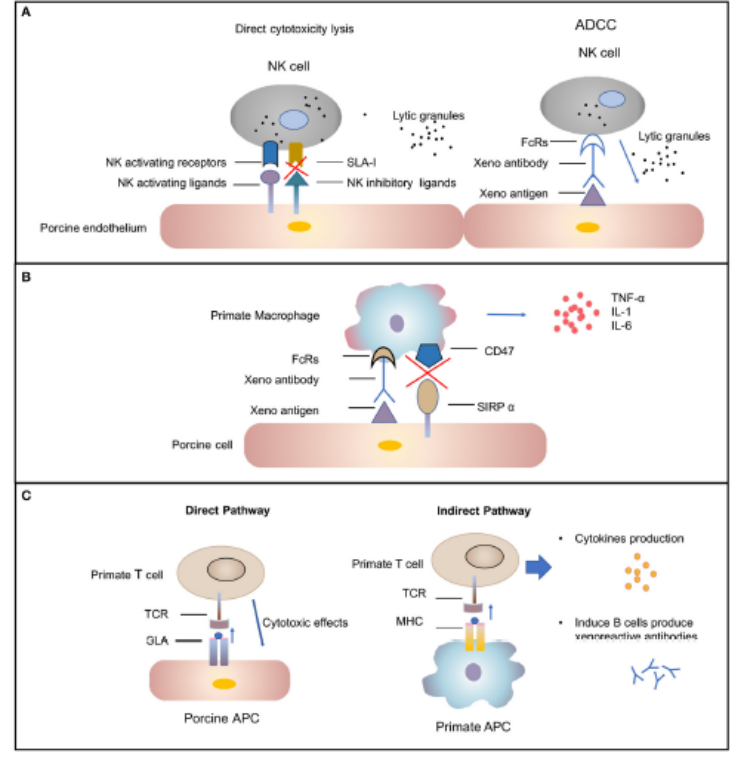
急性细胞排斥反应由固有和适应性免疫介导,包括NK细胞、巨噬细胞、T细胞等。其中,NK细胞通过直接NK细胞毒性或抗体依赖性细胞毒性介导异种移植排斥反应。巨噬细胞通过调节适应性免疫和直接细胞毒性介导异种移植排斥反应,巨噬细胞可通过产生促炎性细胞因子TNF-α、IL-1和IL-6来产生毒性作用,信号调节蛋白(SIRP-a)-CD47信号通路是巨噬细胞的重要负性通路。T细胞通过直接和间接途径被激活,T细胞活化需要两个信号:第一信号由T细胞受体与抗原呈递细胞(MHC)上的抗原肽-MHC复合物结合启动,第二信号由T细胞和MHC间共刺激分子CD40-CD154、CD28-CD80/86作用产生的共刺激信号启动。(图1)
图1.A.NK细胞介导的排斥反应;B.巨噬细胞介导的排斥反应;C.T细胞介导的排斥反应
异种移植的治疗进展3-5
异种移植的治疗进展主要包括敲除异种移植反应性抗原基因、抑制细胞排斥反应、导入人补体调节蛋白(hCRPs)及人类凝血调节蛋白(hTBM)。
最常见的基因敲除是是GGTA1基因的敲除(GTKO),此外还有GGTA1/CMAH、GGTA1/B4GalNT2和GGTA1/CMAH/B4GalNT2双基因或三基因敲除(表1)。
抑制细胞排斥反应可通过阻断SIRPa-CD47、CD40-CD154、B7-CD28等的共刺激信号通路,如抗CD40抗体、抗CD154抗体可阻断CD40-CD154信号通路,人CTLA4-免疫球蛋白(hCTLA4-Ig)可阻断B7-CD28的信号通路,以及经hCD47 、hCTLA4-Ig转染的转基因猪(表1)。还有抗炎症因子的抗体如抗IL-6抗体。
表1.异种移植转基因猪
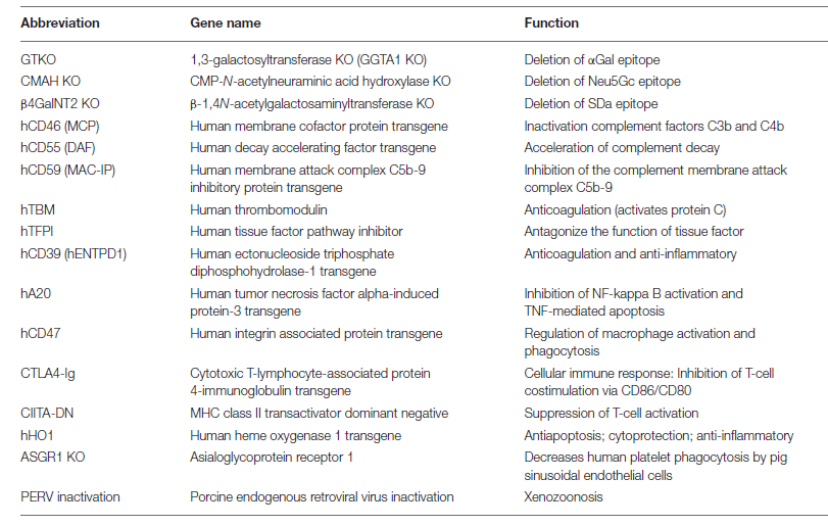
另外,将人CRPs(hCRPs)(如CD46、CD59和CD55)导入猪细胞可抑制补体介导的移植物损伤,研究证明,将hCRPs导入猪细胞还可延长异种移植物存活时间。将hHBM导入猪细胞可抑制凝血酶原活性,延迟凝血时间。
Lifeport机械灌注作为器官移植重要的保存设备,对猪肾脏有保护作用,研究表明,Lifeport机械灌注可保护猪肾脏组织,减轻猪肾脏组织的损害6,在未来异种移植中将起到重要作用。
参考文献
1. 高冰思, 等. 异种移植免疫障碍综述[J]. 现代医药卫生, 2017, 33(7):1032-1035.
2. 张麒, 王建飞. 异种器官移植的进展及展望[J]. 实验动物与比较医学, 2018, 38(6):407-411.
3. Lu T, et al. Xenotransplantation: Current Status in Preclinical Research.Front Immunol.2020 Jan 23;10:3060.
4. Martin Wijkstrom,et al.Renal xenotransplantation: experimental progress and clinical prospects . Kidney Int . 2017;91(4):790-796.
5. Hawthorne WJ, et al. Xenotransplantation literature update, November/December 2020.Xenotransplantation. 2021;28(2):e12674.
6. 谢大炜, 等. 持续低温灌注设备LifePort对离体猪肾组织结构的影响[J]. 中华器官移植杂志, 2016(37):117-121.
扫码关注我们
微信号|Tx新方案
健耕医药,专注移植产业



