
抗体介导的排斥反应是影响移植物长期存活的主要因素,因此一直是近年来移植届关注的热点,美国移植杂志6月专题增刊,发表5篇综述,从动物模型到临床,从机制到防治等多角度阐述了这一问题。
背 景
当前,短期肾移植和患者存活率较高(1 年 > 95%)且急性排斥反应率较低 (5%-15%),但长期肾移植存活率仍不理想。近年来,人们认识到抗体介导的排斥反应 (ABMR) 经常参与早期和晚期同种异体肾移植物丢失,并在该领域进行了大量研究。但美国FDA在其 2017 年关于肾移植 ABMR 公共研讨会的总结中指出,“目前尚无 FDA 批准的急性或慢性 ABMR 治疗方法。与脱敏方案相似,血浆置换或高剂量 IVIG 构成了”标准治疗”,每个中心偏好不同的辅助治疗。所以ABMR 仍然是移植医学面临的主要挑战之一。
本文将总结导致记忆和新发供体特异性抗体 (DSA) 相关性 ABMR 的危险因素、最佳预防策略以及辅助和新兴疗法的进展。
供者特异性抗体(DSA)的风险因素和影响

记忆相关的ABMR

从实体器官移植发展的早期开始,致敏作用已被公认为是成功移植结局的主要障碍。
风险评估工作组在其 2017 年和 2019 年的报告中详尽地总结了移植前风险评估中同种免疫分析在当前的最佳使用,要点是:
(1) 仅通过固相 SAB (单抗原磁珠法)可检测到的低滴度的DSA可引起 ABMR;
(2) 即使在 SAB 未检测到 DSA 的情况下也可存在 B 细胞记忆,可能引起 ABMR;
(3) 移植前预测记忆反应强度。
流式淋巴细胞毒交叉配型阴性但SAB DSA 阳性时ABMR 和移植物丢失的风险均增加。移植后持续进展的DSA 与 ABMR 和移植物丢失的风险增加相关,并且可能在高达50% 的个体中发生。
总之,数据支持在预存 DSA 的情况下,无论检测水平如何,同种免疫记忆均是在 ABMR 和移植物丢失的风险。

dn DSA(新发 DSA) 相关的ABMR

目前临床实践中遇到的最普遍的是与dn DSA相关的ABMR。与dn DSA形成和 ABMR 强相关的因素是 HLA II 类不匹配、年龄较小、TCMR和免疫抑制不足。在这个框架内,医师指导的免疫抑制最小化(由于感染、癌症或药物毒性)和患者依从性差同样是引起 TCMR、dn DSA、ABMR 和移植物丢失的关键因素。
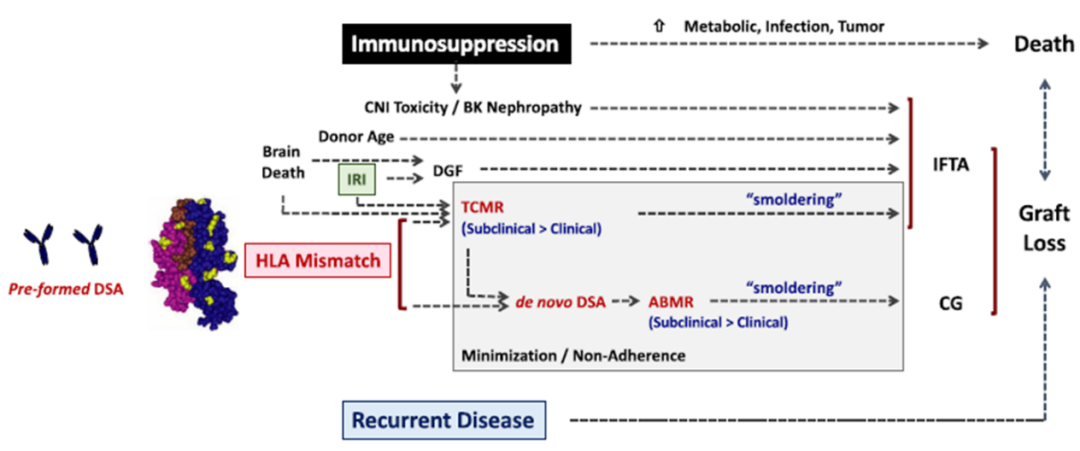
图1 死亡和移植物丢失的机制
(灰色部分代表因免疫抑制最小化和依从性差所致免疫抑制不足造成的免疫反应)
预 防 措 施

记忆相关的ABMR

理想情况下,研究中心可以避免任何可检测的预存 HLA DSA。对于高致敏候选人,可以采用肾脏交换配对和全国的器官共享。无预存SAB DSA的致敏患者的移植结局与未致敏受体相当。然而,等待名单上高致敏(即计算的群体反应性抗体> 99.95%)的候选人罕见DSA 阴性。对于这些个体,应当术前脱敏。

dn DSA(新发 DSA)相关的ABMR

维持足够的免疫抑制强度(尤其是包含CNI的方案)是预防TCMR和新生DSA的关键策略,但由于CNI 对肾脏受者的副作用(例如 eGFR 受损/肾毒性、神经毒性和胃肠道毒性),目前正在积极寻找替代方案。这种策略的关键是维持控制同种免疫应答的有效性,特别是在预防dn DSA形成和 ABMR 发展方面。
贝拉西普的共刺激阻断可以通过改变生发中心反应来预防 ABMR,在其早期研究,与环孢素或他克莫司相比,贝拉西普与新发 DSA 形成显著减少相关。
HLA-II的匹配降低了TCMR,dn DSA,ABMR,移植肾肾小球疾病和移植物丢失的风险.尤其是HLA-DQ/DQ的匹配尤为重要。近年新的观点认为分子水平(比如氨基酸水平)的配型更为精准。例如HLA-DR/DQ的分子水平的匹配可以使受者使用低剂量的CNI而不发生免疫反应。从而可以使免疫抑制方案个体化。
治 疗 措 施
目前尚无 FDA 批准的 ABMR 疗法 ,而且早期和晚期 ABMR 的表型不同,治疗反应性和结局也不同。鉴于这些限制,TTS于 2019 年召开了一个专家共识工作组会议,制定了 ABMR 的推荐治疗方法。

早期活动性 ABMR(移植< 30 天)与DSA 相关

TTS 工作组与FDA 研讨会一致,建议将血浆置换、IVIg 和皮质类固醇的联合作为标准治疗,以去除循环DSA 和/或减少 DSA 生成。
在 FDA 研讨会中提到的“每个中心偏好不同的辅助治疗”,被 TTS 工作组认为是有争议的,但在急性移植物丢失风险较高的情况下,可能需要辅助治疗:包括利妥昔单抗(抗CD20单抗)、补体抑制剂(如 eculizumab)和脾切除术。

晚期活动性和慢性活动性 ABMR(移植后 > 30 天)
对于预存DSA 相关的晚期活动性 ABMR,TTS 工作组的共识推荐仍然是血浆置换、IVIg 和皮质类固醇,可以考虑利妥昔单作为辅助治疗。
然而,一旦记忆相关的ABMR演变为慢性活动型,考虑到免疫抑制过度的风险(没有任何药物的有效性证明)工作组倾向于考虑支持治疗,同时优化基础免疫抑制方案(即他克莫司谷值>5.0 ng/mL)。
dn DSA相关的活动性和慢性活动性 ABMR 通常是TCMR/ABMR 混合表型,主要归因于免疫抑制不足,通常难以逆转。因此,TTS 工作组建议优化基础免疫抑制,并治疗TCMR。血浆置换、IVIg 和利妥昔单抗的治疗证据被认为太低,不推荐作为标准治疗,但可考虑作为辅助治疗。
辅助和新兴治疗措施
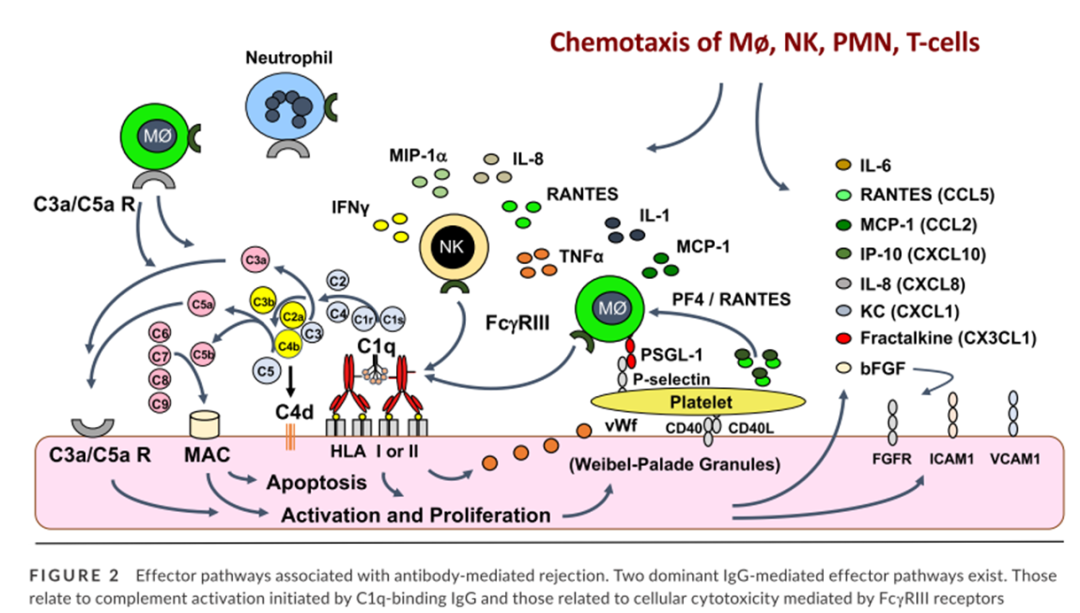
图2 ABMR的效应机制

抗补体

在 ABMR 中,补体途径是通过补体依赖性细胞毒性(如C5-C9 膜攻击复合物)和 C3a/C3b/C5a 介导的内皮活化/炎性细胞趋化导致组织损伤的主要效应途径。
在一项 eculizumab(抗C5单抗)治疗dn DSA相关 ABMR 的初步 RCT研究中,肾功能有稳定的趋势,但内皮活化相关的基因表达未受影响。这可能是因为 C5 被抑制使早期促炎性补体介质(例如C3a/C3b)无对抗作用,而后者可激活内皮。
巴黎小组在标准治疗(即血浆置换、IVIg、利妥昔单抗)无效的活动性 ABMR 患者中进行了一项为期 6 个月的 C1 抑制剂 (INH) + IVIg 的前瞻性、单臂研究,结果显示肾功能显著改善,同时安全性尚可。另外,一项美国前瞻性、多中心、双盲、安慰剂对照 RCT 初探性研究,比较了 C1-INH 与安慰剂作为血浆置换的辅助治疗,同样观察到了肾功能改善和更少的移植肾小球病趋势。
这些研究充分表明了抗补体的潜在疗效,但仍需正式大规模的RCT进一步研究补体抑制疗效。

抗IL-6治疗

在 ABMR 中,IL-6可以 促进B细胞发育和成熟为浆细胞,产生靶向同种异体移植物的DSA。
其致病作用来源于以下一些证据:(1)在一个非对照的肾移植受体队列研究中,难治性慢性活动性 ABMR 患者每月输注托珠单抗 (TCZ-anti-IL-6R mAb) 降低了 DSA 和微血管炎症,并稳定了eGFR;(2) 每月 IVIg + TCZ 脱敏治疗 6 个月,肾移植率为 50%。总之,在移植前和移植后进行抗IL-6治疗降低了 DSA ,预防了ABMR的发生。
目前TCZ 3 期试验尚未进行,但FDA 新药 clazakizumab (Claza-anti-IL6 mAb) 正在慢性活动性 ABMR 患者中进行安慰剂对照、多中心 3 期试验。
我们还需探索什么?

HLA 与非 HLA 抗体的相对重要性

越来越多的研究认为,非 HLA 遗传错配与移植物丢失相关,与 HLA 错配无关。除了检测非 HLA 抗体的能力,还有许多问题仍然存在:非 HLA ABMR 的存在程度如何?非 HLA ABMR 的预后结局是什么?Senev 等的论文提示,早期非 HLA ABMR 的结局与无 ABMR 的肾移植受者相似。非 HLA ABMR 的最佳治疗方法是什么,对“标准治疗”的反应是否优于或差于 HLA DSA ABMR?显然,关于非 HLA 相关 ABMR 还有很多需要研究的地方。

TCMR 与 ABMR 的相对作用

通常,晚期活动性和慢性活动性 ABMR被认为是TCMR/ABMR 混合表型,由此产生了一个问题, 即TCMR在导致移植物丢失中所起作用的问题。仅靶向 DSA、浆细胞和 B 细胞是否足够?是否还需要考虑 治疗TCMR的新方法?尽管 2017 年 Banff 工作组已经认识到慢性活动性 TCMR 是导致移植物丢失的原因,但尚不清楚当前的 TCMR 治疗方法在移植晚期是否足够有效。新策略(如抗 IL6/IL-6R 治疗)具有调节 B 细胞、浆细胞和 T 细胞的能力,也许会有更优的治疗潜力。

CDC vs 抗体依赖性细胞毒性 (ADCC) 效应通路的相对重要性

除了靶向抗体的产生外,还要阻断与 IgG 介导的 C1q 结合相关的 CDC 效应通路。然而,与 IgG FcγR (FcγR) 介导相关的 ADCC 可能在 ABMR 中同样发挥作用,因为 NK 细胞基因转录增加,MVI(微血管炎症)显示表达 FcγR 的 NK 细胞和巨噬细胞增加(图 2)。支持 DSA FcγR 介导的 MVI 在 ABMR 中作用的证据来自最近 FcγRIII 基因多态性的 SNP 分析。在本研究中,尽管未观察到肾功能差异,但FcγRIIIA 高亲和力变异体纯合子个体具有更多的 MVI 和更高的 ABMR 趋势。
越来越多的证据表明,非补体介导的同种异体移植物损伤可能在 ABMR 相关移植物丢失中发挥重要作用。因此,靶向 ABMR FcγR 介导的 MVI 或与 MVI 相关的细胞(即 NK 细胞和/或巨噬细胞)的策略需要进一步研究。
推移君插话
在过去的十年里,ABMR相关领域开展了大量研究,但在治疗策略方面依然进展甚微,特别是对于晚期活动性和慢性活动性ABMR。目前的首要策略是通过最佳基线免疫抑制进行预防,维持足够的CNI暴露是预防的关键策略,而共刺激阻断或许可以成为新的非CNI预防策略。从治疗的角度来看,补体抑制剂和IL-6 / IL-6R阻断的一些研究数据表现出了很大的潜力。总之,许多问题仍未得到解答,预防和治疗ABMR的研究前景依然广阔。
参考文献:
Am J Transplant. 2020 Jun;20 Suppl 4:12–22.
DOI: 10.1111/ajt.15859
PMID:32538535
文章转载自:优医Online微信号



