器官短缺是移植领域世界性难题,是制约器官移植发展的重要瓶颈。为应对供器官短缺,越来越多的边缘器官应用于临床,其中包括了来源于感染致病微生物的供体。
一方面,为避免微生物通过移植器官传播给受者,相当数量的供器官被弃用,加剧了器官的短缺。另一方面,感染器官的利用虽然增加了器官来源,但是,此类器官不恰当的使用会给移植受者带来潜在的风险,轻者延长住院时间,加重医疗负担,重者导致移植物的丢失,甚至危及生命。
3月18日国际移植领域顶级期刊《美国器官移植杂志》在线发表了题为“Machine perfusion combined with antibiotics prevents donor-derived infections caused by multidrug-resistant bacteria”的论文。
武汉大学中南医院王彦峰教授团队实验研究证实,在器官体外运输和保存期间,短暂机械灌注(MP)联合抗生素(AB)的治疗,能在移植前有效清除供肾内感染的耐药细菌。该策略突破了使用感染供器官的瓶颈,不仅扩大了供体池,而且保障了肾移植手术的安全。
静态低温冷保存技术(SCS)使用了半个多世纪,迄今仍然是标准器官保存的金标准。伴随边缘器官在临床上越来越多的使用,其缺陷日益突出。本世纪以来,随着的科学技术的快速发展,MP成为当前器官移植领域的研究热点。
该技术在客观评估器官质量和修复器官损伤方面的优势得到了大量临床研究的证实,但是,对于如何利用该技术治疗感染器官缺乏系统的了解。针对供体感染最多的大肠杆菌,和临床上危害最大的多耐肺炎克雷伯杆菌,王彦峰团队利用成熟的低温机械灌注(HMP)、常温机械灌注(NMP)技术和肾脏移植方法,在动物感染模型开展了系统的研究,得出如下结论。
1 、 细菌的数量、种属和感染途径是决定细菌在不同器官分布的关键因素,这为个体化精准使用器官提供了理论依据(图1);


图1.供体细菌分布:A和C为大肠杆菌在不同器官细菌培养菌量和细菌负荷分布;B和D为耐碳青霉烯类肺炎克雷伯菌(CRKP)在不同器官细菌培养菌量和细菌负荷分布
2、 在器官灌洗液或静态冷保存液中加入抗生素对器官内的细菌没有治疗效果(图2A、B);
3、 在HMP或NMP中加入足量的抗生素,灌注3小时,足以杀灭供肾内的细菌(图2A、B、E、F);
4、 与SCS相比,MP可以将肾组织内的抗生素浓度提高8-10倍,保证了杀菌效果,同时,避免了对其它器官的副作用。值得一提的是简单易行的HMP与NMP同样有效(图2A、B、E、F);
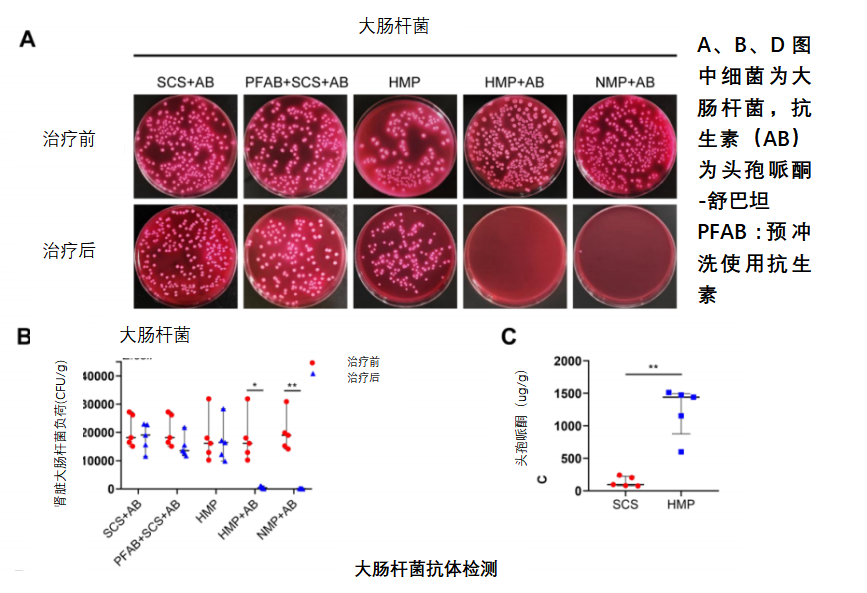
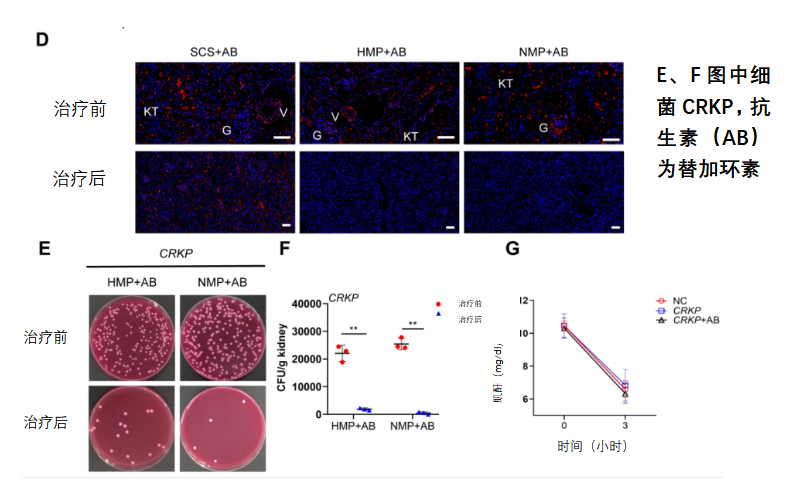
图2.SCS+AB组、HMP+AB组、NMP+AB组对供肾大肠杆菌、CPKP细菌作用的比较:A供肾大肠杆菌培养;B.供肾大肠杆菌细菌负荷;C.头孢哌酮浓度;D供肾大肠杆菌特异性抗体鉴定;E.供肾CRKP细菌培养;F供肾CRKP细菌负荷;G.体外灌注液中外源性肌酐水平
5、 移植细菌感染器官的风险极高,会导致吻合口出血、全身重度感染和受体的死亡(图3);
6、 在大量使用免疫抑制剂受者,三小时的低温机械灌注治疗足以有效预防供器官来源细菌的感染。

图3. SCS+AB组和HMP+AB组接受CRKP感染供肾术后受体情况:A.试验流程:感染CRKP供肾经SCS组+AB或HMP+AB治疗3h后移植,96h解剖受体;B. 治疗后的感染肾脏(移植循环开放前),治疗后移植的感染肾脏(移植循环开放后)C.肾移植4天后,SCS + AB组观察到腹部感染、吻合口出血,HMP+AB组肾移植物状况良好;D.肾移植后SCS+AB组体重变化;E. 肾移植后HMP+AB组体重变化;F.SCS+AB组肾移植4天后组织学,可见血管和肾小球周围炎性细胞大量浸润(黑色箭头);G. HMP+AB组肾移植4天后组织学,移植肾仅有轻度或几乎无炎性细胞浸润
武汉大学中南医院博士生梁涵和张鹏为本文的共同第一作者,王彦峰教授为本文的通讯作者。该研究在动物模型中验证了这一策略的可行性、安全性和有效性,为进一步的多中心随机对照临床试验奠定了基础。机械灌注联合抗生素的策略不仅适用于肾脏移植,同样适合于肺脏和肝脏等器官移植,具有广泛的应用前景。
原文链接:
https://pubmed.ncbi.nlm.nih.gov/35303398/


